電気分解の物質を判断し、分子モデルを思考する<思考力、判断力>(2020年福井)
- 「水300gに水酸化ナトリウムを加えて、2%の水酸化ナトリウム水溶液を作るためには水酸化ナトリウムは水酸化ナトリウムを何g必要とするか。小数第2位を四捨五入して小数第一位まで求めなさい。」
- 「30%の塩酸10gを水で薄めて5%の塩酸にしたい。水を何g加えればよいか」
- 電気分解の結果
- 電気分解は気体の性質と同時に出題
- 電気分解のようすのモデル
- 中学レベルを超える問題が出題される日本海側
- 入試問題攻略法
何を電気分解したのかを判断する
エタノールと水の混合物,塩酸,塩化銅水溶液,砂糖水,水酸化ナトリウム水溶液の5種類の液体を用いて,次の実験を行った。あとの問いに答えよ。
5種類の液体を電気分解できるものと出来ないものに分けることができる
電解質水溶液・・・塩酸、塩化銅水溶液、水酸化ナトリウム水溶液
ということで、5種類の液体をまず2種類に分類する判断力を問う問題がある。
当然テスト問題では「非電解質溶液を選びなさい」という問題が出題されるわけであるが、このようにストレートに聞くと簡単な問題になるので、問題は
「この5種類の液体のうち、電極の周りに変化が見られなかった液体は何か。すべて選びなさい」
というように、遠回しに聞くことで問題をむずかしくさせている。
水溶液の問題では、液体の濃度に関する問題が出題されることが多い。
2020年山口では
「水300gに水酸化ナトリウムを加えて、2%の水酸化ナトリウム水溶液を作るためには水酸化ナトリウムは水酸化ナトリウムを何g必要とするか。小数第2位を四捨五入して小数第一位まで求めなさい。」
水酸化ナトリウムをxgとすると、水溶液の質量が 300+xになる。
「2%の水酸化ナトリウム水溶液300g作りたい。水酸化ナトリウムは何g必要か」
という問題によく似ているが。全然違う。
2%の水酸化ナトリウム水溶液300g中に含まれる水酸化ナトリウムの質量は
300×0.02=6gと計算できるが、
求めたいのは
(300+x)×0.02=x なのである。
両辺を100倍して小数を整数にする
(300+x)×2=100x
600+2x=100x
98x=600
x=600÷98
x=6.12g より小数第二位を四捨五入すると 6.1g
このように、ちょっとした一次方程式を解く問題がこの濃度の問題では出ている。
水溶液の質量×%を100でわったもの=溶質
という公式を丸暗記していてすぐに溶ける問題ではないのである。
福井県でも同様に
「30%の塩酸10gを水で薄めて5%の塩酸にしたい。水を何g加えればよいか」
というようにすぐに出すのは難しそうな問題である。
30%→5% で6倍に薄めているから、水溶液は60g、
もともとの水溶液が10gだから、60ー10=50gの水を加えた。
と判断できれば、計算が速い
30%の塩酸10gに含まれている塩化水素が
10×0.30=3g
3gの塩化水素を水に溶かして5%の塩酸にする
これを5%の水溶液にするから10gの塩酸に水をxg加えると 10+x gの水溶液になる。
その中の5%が塩化水素の質量3gになる
水溶液の質量×%を100でわったもの=溶質
(10+x)×0.05=3
両辺を100倍して
(10+x)×5=300
50+5x=300
5x=250
x=50g
加える水は50g
どちらの方が計算として速いか。これが、今、思考力の問題として問われている。
電気分解の結果
炭素を電極として電気分解を行ったところ、電極 のまわりに変化が見られた液体が3種類あった。 右の表は、その3種類の液体で見られた変化につ いてまとめたものである。また,液体 A, 液体 B については電気分解装置を用いて電気分解を行い,発生した気体をそれぞれ集めた。

結果から判断すること
液体Cだけ陰極には固体が付着する。固体が発生するのは塩化銅水溶液
塩化銅水溶液では 陰極(マイナス極)では陽イオンが近づいて、
銅イオン Cu²⁺が マイナスに近づく
Cu²⁺+2e⁻ → Cu
陽極(プラス極)では陰イオン 塩化物イオン Cℓ⁻ が近づく。
2Cℓ⁻ → Cℓ₂+2e⁻
で塩素の気体が発生するが、塩素は水に溶けやすいので、気体として多くとれない。
液体Bは液体Cと同じ気体が陽極から出ている。ということでこれは Cℓ₂
液体Bは塩化物イオンを含み、Cで決定した塩化銅水溶液ではない溶液 塩酸である。
塩酸では 陰極(マイナス極)ではプラスの電気を持った陽イオンが近づく
ここでは 水素イオン H⁺ が近づいて 2H⁺+2e⁻→H₂
となり
H₂の水素発生 気体Xは水素 H₂ 気体Yは塩素 Cℓ₂ 固体Zは銅 Cu
そして、ここまでわかれば、残った液体Aは水酸化ナトリウム水溶液である。
水酸化ナトリウム水溶液での陽極、陰極での化学反応式は難しくて覚えられない
という人でも 陰極が水素 H₂ 陽極がO₂であるということだけは知っておこう。
難しくて覚えられない人は、次の記事を参考にしてね!!
次に出題されるのはイオンと原子
電極に物質が生成することからイオンの存在を知るとともに、イオンの生成が原子の成り立ちに関係することを知ること
これが「学習指導要領」の目指すところなので、当然入試問題では、イオンと原子の関係についての問題が登場する
原子は本来,電気を帯びていない状態にあるが、電子を失ったり受け取ったりすることでイオンになる。 塩素原子から塩化物イオンができるときの説明として正しいものはどれか。最も適当なものを、次のア~エから1つ選んで、その記号を書け。
ア 塩素原子が電子を1個受け取って陽イオンとなる。
イ 塩素原子が電子を1個受け取って陰イオンとなる。
ウ 塩素原子が電子を1個失って陽イオンとなる。
エ 塩素原子が電子を1個失って陰イオンとなる。
入試問題によく出るのは陽イオンのでき方であるが、この問題のように、陰イオンのでき方が出題されることがある。
この問題では答えはすぐにイを選ぶことができる。
2個の塩化物イオンが電子をそれぞれ1つずつ失って、1分子の塩素分子になる
というのを選択する問題の方がこの問題よりも重要で今後増えていくと考えられる。
それも、電極の周辺で起こる反応を電子をe⁻ 塩化物イオンを〇⁻ 塩素原子を〇として電気分解のモデルで答えなさい

答えはアとなる。
電気分解は気体の性質と同時に出題
表の中にある気体 Y の名称を書け。また、その気体の性質として正しいものはどれか。最も適当なものを、次のア~エ から1つ選んで、その記号を書け。
ア 石灰水に通すと石灰水を白くにごらせる。
イ 火のついた線香を入れると線香を激しく燃やす。
ウ マッチの火を近づけると燃える。
エ 湿らせた赤色リトマス紙を青色にする。
気体Yは水素である。
アは二酸化炭素、イは酸素、ウは水素、エはアンモニアの説明であるということを知っている必要がある。答えはウになる。
電気分解のようすのモデル
液体Bで,陰極側と陽極側に集まった気体の体積を比べたところ、気体Xに比べ気体2の方が小さかった。このときの気体のようすを、モデルを使って正しく説明したものはどれか。最も適当なものを、次のア~エから1つ選んで、その記号 を書け。
液体Bということは 陽極に塩素、陰極に水素が発生する。
その量は 塩素:水素=1:1である。
しかし、塩素は水に溶けやすいので粒子の数は少ない
中学校では習わない高校レベルとして「アボガドロの法則」がある。
これは、同じ体積に含まれる気体は気体の種類に関わらず同じ数の粒子が含まれる。
これは中学校の教科書には載っていない。教科書に載っていないことは公立高校の入試問題には出題されないというのがあるのに、この法則を知っていなければこの問題は解けない。
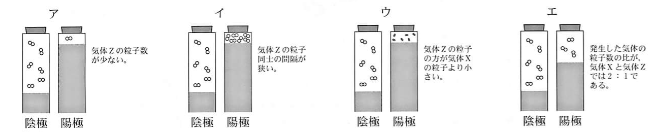
粒子の数を見ると
アイウエの陰極(マイナス極)の水素の粒子は6個ある。
陽極(プラス極)の塩素を見る
アでは体積が小さくて粒子の数が1
イでは体積が小さくて粒子の数が6よりもかなり多い
ウは体積が小さくて粒子の数が6
エは体積が水素の半分で粒子の数が3
塩素は水に溶けやすいので、体積が小さい。アイウのどれか。
さらに、粒子の数が少ないというのを選ぶとアである。
体積が小さい→粒子の数も少ないというのは、アボガドロの法則を知っていないと解けない。この問題は中学レベルではない。
ここで、エのモデルは液体Aを電気分解した結果であるというのは、すぐに見分けることができる。陽極の水素に対して陰極の酸素は水素:酸素=2:1だからである。
しかし、液体Bでアを選択するのは難しい問題に思われる。
中学レベルを超える問題が出題される日本海側
北陸地方の入試問題は中学レベルを超える問題が時々出題されている。この問題もその一つである。福井県の受験生の数が4000人、近県の大阪が40000人と10倍違うので問題に対して中学レベルか高校レベルかを指摘する人が少ないせいかもしれない。中学レベルでは難しいかもしれないが、思考力、判断力があれば解答できるとされている問題が多い。
大阪府は高校入試の問題、正答率を大阪府の教育委員会で公開しているが、福井県は高校入試の問題は、入試が行われた日の地元の新聞各社にだけ公開し、正答率に関しても公表していない。
2021年の全国の公立高校のなかで入手できた都道府県は35県、入手できなかった県は12県である。
新潟、富山、石川、福井、島根、鳥取、山口と日本海に面した多くの県で入手できなかった。これらの県は受験生も少なく、正答率も公表していない。
問題の分析も公表していないところである。これらの県は中学レベルを超える問題を出すことが多い。
入試問題攻略法
2022年はどんな問題が出るのかについて、全国47都道府県のうちいち早く発表したのが、2021年の問題と正答率がホームぺージで発表されていなく、2020年の入試では「2%の水酸化ナトリウム水溶液300gをつくる」という入試問題にわざわざ600÷98という割り切れない計算を受験生にさせて、計算ミスをさせるのを誘発させている山口県である。計算ができなければ解けない問題を出題するのは理科の問題として適切とは思えない。
難関校との点数差をつけるために、いやらしい計算をさせているのであろう。
この山口県の2022年の出題は次のとおりである。
令和4年度山口県公立高等学校入学者選抜・学力検査の出題範囲|山口県
中学校学習指導要領の定める内容とだけ書いてある。
中学校学習指導要領では2022年から「見通しをもって行う」が重視されている。
電気分解の問題では、電解質溶液を使う、電極から発生する物質を求める、電極から発生する物質の性質を答える、電極ではどのようなことが起こっているかをモデルで示すという問題が出るよという見通しをもって問題を解く。ということが求められるのではないだろうか。