【中三応援プログラム】電池の仕組み(2021年岩手県)
電池の仕組みとして
電極に異なる金属を用いる
電解質溶液を使う
新学習指導要領でダニエル電池を学ぶことになったので極版での変化も重要になる。
極版ではイオン式を書けるようにしておきたい
今まで電子の表示が
⊖⊖やeeとかいてあったのが 新学習指導要領で 2e⁻に統一される。
いままで溶液の濃度と電流の大きさは出題されていなかったが、今後は濃度との関係も出題されるかもしれない。
その一つの例として、今回、塩酸の濃度が大きいかどうかが出題されている
塩酸の濃度が大きいほど、亜鉛板が溶けやすくなる。
中学校レベルでは極板間の距離が近いほど電流が大きく流れるというのは学習しない。
極板の面積が大きくなるほど電流が大きくなるというのが今回出題された。
今回の問題のように、仮説を立てて、実験方法を考えるというのがこれから多くなると考えられる。
実験1 電池のしくみと水溶液の関係を調べた。
図1

1 図1のように、蒸留水を入れたビーカーに、電極と して亜鉛板と銅板を入れ、モーターにつないだところ、 モーターは回らなかった。
2食塩水,砂糖水、エタノール水溶液,水酸化ナトリウム水溶液を用意し、それぞれ1と同様の実験をした ところ、食塩水のときと水酸化ナトリウム水溶液のと きにモーターが回り電流が流れたことがわかった。
3うすい塩酸を用意し、1と同様の実験をしたところ、2のときよりモーターがよく回り電 流が流れたことがわかった。
4 3のとき、電極付近で気体が発生し,亜鉛板の表面は少し溶けてざらざらしているのが確 認できた。
実験2で、モーターがよく回ったのは、流れる電流が大きくなったからだと考え、電流を大きくするための条件を調べた。
5 実験を行う前に、電流を大きくする条件について次のように予想した。
予想1 塩酸の濃度を大きくすると、電流が大きくなるのではないか。
予想2 塩酸に入れる亜鉛板と銅板の面積を大きくすると、電流が大きくなるのではないか。
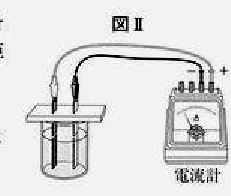
6 ビーカーAに濃度 0.1%の塩酸を入れ、図Ⅱのように銅板を 電流計の+端子に,亜鉛板を一端子に接続し、塩酸に入れる亜 鉛板と銅板の面積を9cm²として電流を測定した。
7 ビーカーBに濃度1%の塩酸を入れ、塩酸に入れる亜鉛板と銅板の面積を18cm²とし、6と同様に電流を測定した。
8 6.7の結果を表にまとめた。

金属の性質
(1) 次のア~エのうち、亜鉛と銅に共通の性質として正しいものはどれですか。一つ選び、その記 号を書きなさい。
ア磁石に引きつけられる。
鉄やニッケルの性質であり、金属の性質ではない
イたたくとうすく広がる。
たたくと薄く広がる(展性)
引っ張ると延びる(延性)
電気をよく通す(電気伝導性がある)
熱を伝える(熱伝導性が大きい)
金属光沢がある
これらが金属には自由電子があるために共通して持つ。
ウ空気中で激しく燃える。
これは、マグネシウムなどのイオン化傾向の大きい物質の性質である。
イオン化傾向の大きい物質は空気中で燃焼する。
燃焼とは光や熱を出して激しく酸素と結びつく反応のこと
エ エタノールによく溶ける。
金属はエタノールにはとけない
電解質の水溶液だから
(2) 2で、食塩水のときと水酸化ナトリウム水溶液のときに、電流が流れ、モーターが回ったのはなぜですか。簡単に書きなさい。
純水は電気を通しにくい
砂糖水では水溶液中に電離しているイオンがない
食塩水は電離して陽イオンのナトリウムイオンと陰イオンの塩化物イオンがある
水酸化ナトリウム水溶液は陽イオンのナトリウムイオンと陰イオンの水酸化物イオンがある、
イオンがある水溶液は電気を流す。化学電池は負極と正極の間で電気が流れる必要がある。
電解質水溶液であるから
(3) 4で、極板の表面では気体の発生が見られました。次のア~エのうち、発生した気体の特徴として正しいものはどれですか。一つ選び、その記号を書きなさい。
ア火を近づけると一瞬で燃焼する。
イ 空気中の約78%をしめ、水に溶けにくい。
ウ、特有の刺激臭があり、殺菌や悪白に使われる。
エ ものを燃やすはたらきがあるが、そのものは燃えない。
発生した気体は水素である。爆鳴で激しく燃える。というのを選ぶ
ところがそう書いてある選択肢がない
そこで最も適当なものを選ぶ
イは窒素の説明
ウは塩素の説明
エは酸素の説明
であることから、一瞬で燃えるというのを爆鳴と判断し1を選ぶ
(4) 4で,亜鉛板が溶ける化学変化をe(電子)を用いたモデルで表すとどうなりますか。(例)を参考にして、下の( )に適当なイオン式を書きなさい。
(例)塩化物イオンが電子を放出して塩素分子になる反応のモデル
2Cl⁻→ Cl₂ +2e⁻
2021年の新学習指導要領から電子の表記が e⁻にかわったので、それに合わせた
出題が 亜鉛原子が水溶液で 亜鉛イオン(陽イオン)になって、電子を放出する
Zn→Zn²⁺+2e⁻
例で書かれてあるのでは電池ではなく電気分解で陽極で起こる反応である
これを参考にして電池の式を書くというのは難しいかもしれない。
仮説が正しいことを確認する方法
(5) 5の予想について、6~8では予想が正しいことを確認することはできません。2つの予想のうち、予想が正しいことを確認するためには、どのような実験をして、どのような結果が得ら れればよいですか。簡単に書きなさい。ただし、塩酸の濃度や亜鉛板と銅板の面積は、実験2と 同じものを用いるものとします。
この実験では、塩酸の濃度と極板の面積を同時に変えたので、極板の面積が大きくなったから電流が大きくなったのか濃度が大きくなったかわからない。
塩酸の濃度を固定して、極板の面積を変えて電流の大きさを調べる。
塩酸の濃度を0.1%、極板の面積を18cm²にして、電流を測定して流れる電流が23mAより小さくなるかどうか調べる。
極板の面積を固定して 塩酸の濃度を変えて、電流の大きさを調べる。
塩酸の濃度を1%、極板の面積を9cm²にして、電流を測定して流れる電流が5mAより大きくなるかどうか調べる。