【中三応援プログラム】<思考力判断力が必要な問題>酸化銅の還元(2021年山口)
今日は2021年の山口県の問題である。酸化銅の還元に関する問題で炭素と酸化銅の反応比を3:8と出せる理由を考えさせる問題になっている。
この問題はかなり難しい問題ではないだろうか。
Kさんのクラスでは,酸化銅と炭素の反応について調べるため,1班から5班に分かれて,次の実験を行った。あとの(1)~(3)に答えなさい。
[実験]
1 空の試験管 A の質量をはかった。
2 班ごとに, 酸化銅 6.00gと表1に示した質量の炭素をはかりとり,よく混ぜ合わせた後,空の試験管Aに入れた。
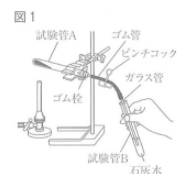
3 図1のように、試験管Aにゴム栓をし、ゴム管やピンチコック,ガラス管をつけ,ガラス管の先を、石灰水が入った試験管Bに入れた。
4 ピンチコックを開け,ガスバーナーで十分に加熱すると,気体が発生し、石灰水が白くにごった。
5 気体が発生しなくなった後,試験管A内の物質の図1 ようすを観察した。
6 石灰水が入った試験管Bからガラス管を取り出し, 加熱を止め, ピンチコックを閉めた。
7 試験管A内の物質が冷めたことを確認し、ゴム栓をはずして,物質の入った試験管Aの質量をはかった。
8 「1ではかった質量」と「7ではかった質量」の差から, 加熱後の試験管A内の物質の質量を計算で求めた。 各班の実験結果を,表1にまとめた。
化学反応の名称
(1) [実験]の1では,酸化銅から酸素をうばう化学変化が起きた。このように,酸化物から酸素をうばう化学変化を何というか。書きなさい。
これは、定番の問題である。静岡など酸化銅の問題が出題されるとこれがよく聞かれる。
酸素を奪う反応を 還元 という、
還元は水素と結びつく反応も還元という
酸素と結びつく反応を酸化という。
酸化銅の反応後にやること
(2) [実験]の6において、加熱後にピンチコックを閉めなければならないのはなぜか。 その理由を簡潔に述べなさい。
加熱をやめる前にやらなくてはいけないこと
石灰水の入った試験管Bからガラス管をだす。
その理由
石灰水の逆流を防ぐため
ピンチコックを閉める
試験管A内の銅が空気中の酸素と反応するのを防ぐため
試験管A内に空気中の酸素が入るのを防ぐため
せっかくこの実験で酸化銅を炭素で還元しているのに空気中の酸素と反応して酸化銅に戻ったら実験結果がうまく出ない。
加熱後、火を止めても熱いうちは銅が空気中の酸素と反応するのでそれを防がなくてはならない。

(3) KさんとLさんは,実験の結果をもとに考察し, 「炭素の質量」と「炭素が酸化銅からうばった酸素の質量」の比について,次の のような会話をした。下のア, イに答えなさい。
Kさん: 「炭素の質量」と「炭素が酸化銅からうばった酸素の質量」の比を計算してみたら3:8になったけれど,Lさんの考えを教えてくれないかな。
Lさん: 私は、3班で用いた炭素の質量と,用いた炭素が酸化銅からうばった酸素の質量を比べて,3: 8 を導いたよ。用いた炭素が酸化銅からうばった酸素の質量は,酸化銅の質量から,3班の( )を引くと、求めることができたよ。Kさんは、どう考えたの。
Kさん: 私は,2班と3班の実験結果に注目して計算したよ。
Lさん: 2班では,酸化銅がまだ残っていると思うけれど,どうやって計算したのかな。
Kさん: 3班の実験と比べることで,2班の実験では,酸化銅をすべて反応させるために,あと 0.15 g の炭素が必要だったことがわかるよ。
Lさん: なるほど。2班と3班の実験後の質量の差を考えると,計算ができそうだね。
Kさん: はい。2班と3班の実験後の試験管A内の物質の質量の差である 0.40gは,0.15 g の炭素がうばうことができる酸素の質量になると思うよ。
Lさん: 確かにそうだね。2つの班の実験結果を比較するという,Kさんの考え方はおもしろいね。2班と3班の組み合わせ以外でも,質量の比を計算できる 班の組み合わせはあるのかな。
アにあてはまる語句を,次の1~4から1つ選び,記号で答えなさい。
1 空の試験管 Aの質量
2 加熱後の物質の入った試験管 A の質量
3 加熱前の試験管 A内の物質の質量
4 加熱後の試験管 A内の物質の質量
反応前の試験管A内に最初に酸化銅6.0gと炭素0.45gを入れてある。
反応後の試験管A内には
1班、2班は 未反応の酸化銅(黒色)と銅(赤色)
3班には 銅のみ
4班、5班には 銅と未反応の炭素
7で試験管を含む反応後の質量を量っているので1で求めた試験管の質量を引かないと試験管A内の物質の質量がわからない。その量が8の質量である。
ここでは8の質量を選択させる問題だが、8の質量は何に関してのものかがわかっているかという問題である。
選択肢の4 加熱後の試験管A内の質量というのが答えになる。
考察の仕方
イ 下線部について,実験結果から,「炭素の質量」と「炭素が酸化銅からうばった 酸素の質量」の比が 3: 8 であることを計算できる班の組み合わせとして,適切 なものを,次の1~4から1つ選び,記号で答えなさい。ただし,計算に用いる数値 は,表1の実験結果のみとする。
1 1班と2班
2 1班と5班
3 2班と4班
4 4班と5班
1班と2班で考えてみよう。
1班と2班の違いは炭素の量が0.15g多くなると0.40gの質量変化がある。
この質量変化は残った酸化銅が銅に変化した質量である。
1班と5班の違いは炭素の量が0.60g違うと、0.40gの質量変化がある。
この質量変化は1班は酸化銅と銅の混合物 5班は銅と炭素の混合物である・
2班と4班の違いは 1班と5班の違いのように混合物を考える必要がある
4班と5班の違いは炭素の量が0.15g違うと、0.15gの質量変化がある。
この質量変化は過剰に加えている炭素の量である。
このようなことから、1班と2班を比較すると炭素の質量変化とどれだけ酸化銅が反応したかの量を考えることができる。
1班と2班の場合
炭素0.15g:酸化銅0.40=3:8になる。
このほかにも1班と3班の組み合わせでも計算ができる
炭素の質量変化0.30g、酸化銅0.80=3:8
酸化銅が過剰で炭素が不足している場合は、酸化銅と炭素の反応量で比例の関係にある。そのため、比を使って計算することができる。
一方、炭素が過剰にある場合は、残った炭素の量がわかるだけで酸化銅と炭素の反応比はもとめることができない。
答え1